
The carbon cycle is the biogeochemical cycle by which carbon is exchanged among the biosphere, pedosphere, geosphere, hydrosphere, and atmosphere of the Earth. Carbon is the main component of biological compounds as well as a major component of many minerals such as limestone. Along with the nitrogen cycle and the water cycle, the carbon cycle comprises a sequence of events that are key to make Earth capable of sustaining life. It describes the movement of carbon as it is recycled and reused throughout the biosphere, as well as long-term processes of carbon sequestration to and release from carbon sinks.
The carbon cycle was discovered by Antoine Lavoisier and Joseph Priestley, and popularised by Humphry Davy.
Main components
| Pool | Quantity (gigatons) |
|---|---|
| Atmosphere | 720 |
| Ocean (total) | 38,400 |
| Total inorganic | 37,400 |
| Total organic | 1,000 |
| Surface layer | 670 |
| Deep layer | 36,730 |
| Lithosphere | |
| Sedimentary carbonates | > 60,000,000 |
| Kerogens | 15,000,000 |
| Terrestrial biosphere (total) | 2,000 |
| Living biomass | 600 – 1,000 |
| Dead biomass | 1,200 |
| Aquatic biosphere | 1 – 2 |
| Fossil fuels (total) | 4,130 |
| Coal | 3,510 |
| Oil | 230 |
| Gas | 140 |
| Other (peat) | 250 |
The global carbon cycle is now usually divided into the following major reservoirs of carbon interconnected by pathways of exchange:
- The atmosphere
- The terrestrial biosphere
- The ocean, including dissolved inorganic carbon and living and non-living marine biota
- The sediments, including fossil fuels, freshwater systems, and non-living organic material.
- The Earth’s interior (mantle and crust). These carbon stores interact with the other components through geological processes.
The carbon exchanges between reservoirs occur as the result of various chemical, physical, geological, and biological processes. The ocean contains the largest active pool of carbon near the surface of the Earth. The natural flows of carbon between the atmosphere, ocean, terrestrial ecosystems, and sediments are fairly balanced so that carbon levels would be roughly stable without human influence.
Atmosphere

Carbon in the Earth’s atmosphere exists in two main forms: carbon dioxide and methane. Both of these gases absorb and retain heat in the atmosphere and are partially responsible for the greenhouse effect. Methane produces a larger greenhouse effect per volume as compared to carbon dioxide, but it exists in much lower concentrations and is more short-lived than carbon dioxide, making carbon dioxide the more important greenhouse gas of the two.
Carbon dioxide is removed from the atmosphere primarily through photosynthesis and enters the terrestrial and oceanic biospheres. Carbon dioxide also dissolves directly from the atmosphere into bodies of water (ocean, lakes, etc.), as well as dissolving in precipitation as raindrops fall through the atmosphere. When dissolved in water, carbon dioxide reacts with water molecules and forms carbonic acid, which contributes to ocean acidity. It can then be absorbed by rocks through weathering. It also can acidify other surfaces it touches or be washed into the ocean.
Human activities over the past two centuries have significantly increased the amount of carbon in the atmosphere, mainly in the form of carbon dioxide, both by modifying ecosystems’ ability to extract carbon dioxide from the atmosphere and by emitting it directly, e.g., by burning fossil fuels and manufacturing concrete.
In the extremely far future (e.g. 2-3 billion years), the rate at which carbon dioxide is absorbed into the soil via the carbonate–silicate cycle will likely increase due to expected changes in the sun as it ages. The expected increased luminosity of the Sun will likely speed up the rate of surface weathering. This will eventually cause most of the carbon dioxide in the atmosphere to be squelched into the Earth’s crust as carbonate. Though volcanoes will continue to pump carbon dioxide into the atmosphere in the short term, it will not be enough to keep the carbon dioxide level stable in the long term. Once the carbon dioxide level falls below 50 parts per million, C3 photosynthesis will no longer be possible. This is expected to occur about 600 million years from now.
Once the oceans on the Earth evaporate in about 1.1 billion years from now, plate tectonics will very likely stop due to the lack of water to lubricate them. The lack of volcanoes pumping out carbon dioxide will cause the carbon cycle to end between 1 billion and 2 billion years into the future.
Terrestrial biosphere
The terrestrial biosphere includes the organic carbon in all land-living organisms, both alive and dead, as well as carbon stored in soils. About 500 gigatons of carbon are stored above ground in plants and other living organisms, while soil holds approximately 1,500 gigatons of carbon. Most carbon in the terrestrial biosphere is organic carbon, while about a third of soil carbon is stored in inorganic forms, such as calcium carbonate. Organic carbon is a major component of all organisms living on earth. Autotrophs extract it from the air in the form of carbon dioxide, converting it into organic carbon, while heterotrophs receive carbon by consuming other organisms.
Because carbon uptake in the terrestrial biosphere is dependent on biotic factors, it follows a diurnal and seasonal cycle. In CO2 measurements, this feature is apparent in the Keeling curve. It is strongest in the northern hemisphere because this hemisphere has more land mass than the southern hemisphere and thus more room for ecosystems to absorb and emit carbon.
Carbon leaves the terrestrial biosphere in several ways and on different time scales. The combustion or respiration of organic carbon releases it rapidly into the atmosphere. It can also be exported into the ocean through rivers or remain sequestered in soils in the form of inert carbon. Carbon stored in soil can remain there for up to thousands of years before being washed into rivers by erosion or released into the atmosphere through soil respiration. Between 1989 and 2008 soil respiration increased by about 0.1% per year. In 2008, the global total of CO2 released by soil respiration was roughly 98 billion tonnes, about 10 times more carbon than humans are now putting into the atmosphere each year by burning fossil fuel (this does not represent a net transfer of carbon from soil to atmosphere, as the respiration is largely offset by inputs to soil carbon). There are a few plausible explanations for this trend, but the most likely explanation is that increasing temperatures have increased rates of decomposition of soil organic matter, which has increased the flow of CO2. The length of carbon sequestering in soil is dependent on local climatic conditions and thus changes in the course of climate change.
Ocean
The ocean can be conceptually divided into a surface layer within which water makes frequent (daily to annual) contact with the atmosphere, and a deep layer below the typical mixed layer depth of a few hundred meters or less, within which the time between consecutive contacts may be centuries. The dissolved inorganic carbon (DIC) in the surface layer is exchanged rapidly with the atmosphere, maintaining equilibrium. Partly because its concentration of DIC is about 15% higher but mainly due to its larger volume, the deep ocean contains far more carbon—it’s the largest pool of actively cycled carbon in the world, containing 50 times more than the atmosphere—but the timescale to reach equilibrium with the atmosphere is hundreds of years: the exchange of carbon between the two layers, driven by thermohaline circulation, is slow.
Carbon enters the ocean mainly through the dissolution of atmospheric carbon dioxide, a small fraction of which is converted into carbonate. It can also enter the ocean through rivers as dissolved organic carbon. It is converted by organisms into organic carbon through photosynthesis and can either be exchanged throughout the food chain or precipitated into the oceans’ deeper, more carbon-rich layers as dead soft tissue or in shells as calcium carbonate. It circulates in this layer for long periods of time before either being deposited as sediment or, eventually, returned to the surface waters through thermohaline circulation. Oceans are basic (~pH 8.2), hence CO2 acidification shifts the pH of the ocean towards neutral.
Oceanic absorption of CO2 is one of the most important forms of carbon sequestering limiting the human-caused rise of carbon dioxide in the atmosphere. However, this process is limited by a number of factors. CO2 absorption makes water more acidic, which affects ocean biosystems. The projected rate of increasing oceanic acidity could slow the biological precipitation of calcium carbonates, thus decreasing the ocean’s capacity to absorb carbon dioxide.
Geosphere
The geologic component of the carbon cycle operates slowly in comparison to the other parts of the global carbon cycle. It is one of the most important determinants of the amount of carbon in the atmosphere, and thus of global temperatures.
Most of the earth’s carbon is stored inertly in the earth’s lithosphere. Much of the carbon stored in the earth’s mantle was stored there when the earth formed. Some of it was deposited in the form of organic carbon from the biosphere. Of the carbon stored in the geosphere, about 80% is limestone and its derivatives, which form from the sedimentation of calcium carbonate stored in the shells of marine organisms. The remaining 20% is stored as kerogens formed through the sedimentation and burial of terrestrial organisms under high heat and pressure. Organic carbon stored in the geosphere can remain there for millions of years.
Carbon can leave the geosphere in several ways. Carbon dioxide is released during the metamorphism of carbonate rocks when they are subducted into the earth’s mantle. This carbon dioxide can be released into the atmosphere and ocean through volcanoes and hotspots. It can also be removed by humans through the direct extraction of kerogens in the form of fossil fuels. After extraction, fossil fuels are burned to release energy and emit the carbon they store into the atmosphere.
Deep carbon cycle
Although deep carbon cycling is not as well-understood as carbon movement through the atmosphere, terrestrial biosphere, ocean, and geosphere, it is nonetheless an incredibly important process. The deep carbon cycle is intimately connected to the movement of carbon in the Earth’s surface and atmosphere. If the process did not exist, carbon would remain in the atmosphere, where it would accumulate to extremely high levels over long periods of time. Therefore, by allowing carbon to return to the Earth, the deep carbon cycle plays a critical role in maintaining the terrestrial conditions necessary for life to exist.

Furthermore, the process is also significant simply due to the massive quantities of carbon it transports through the planet. In fact, studying the composition of basaltic magma and measuring carbon dioxide flux out of volcanoes reveals that the amount of carbon in the mantle is actually greater than that on the Earth’s surface by a factor of one thousand. Drilling down and physically observing deep-Earth carbon processes is evidently extremely difficult, as the lower mantle and core extend from 660 to 2,891 km and 2,891 to 6,371 km deep into the Earth respectively. Accordingly, not much is conclusively known regarding the role of carbon in the deep Earth. Nonetheless, several pieces of evidence—many of which come from laboratory simulations of deep Earth conditions—have indicated mechanisms for the element’s movement down into the lower mantle, as well as the forms that carbon takes at the extreme temperatures and pressures of said layer. Furthermore, techniques like seismology have led to a greater understanding of the potential presence of carbon in the Earth’s core.
Carbon in the lower mantle
Carbon principally enters the mantle in the form of carbonate-rich sediments on tectonic plates of ocean crust, which pull the carbon into the mantle upon undergoing subduction. Not much is known about carbon circulation in the mantle, especially in the deep Earth, but many studies have attempted to augment our understanding of the element’s movement and forms within said region. For instance, a 2011 study demonstrated that carbon cycling extends all the way to the lower mantle. The study analyzed rare, super-deep diamonds at a site in Juina, Brazil, determining that the bulk composition of some of the diamonds’ inclusions matched the expected result of basalt melting and crytallisation under lower mantle temperatures and pressures. Thus, the investigation’s findings indicate that pieces of basaltic oceanic lithosphere act as the principle transport mechanism for carbon to Earth’s deep interior. These subducted carbonates can interact with lower mantle silicates, eventually forming super-deep diamonds like the one found.

However, carbonates descending to the lower mantle encounter other fates in addition to forming diamonds. In 2011, carbonates were subjected to an environment similar to that of 1800 km deep into the Earth, well within the lower mantle. Doing so resulted in the formations of magnesite, siderite, and numerous varieties of graphite. Other experiments—as well as petrologic observations—support this claim, indicating that magnesite is actually the most stable carbonate phase in most part of the mantle. This is largely a result of its higher melting temperature. Consequently, scientists have concluded that carbonates undergo reduction as they descend into the mantle before being stabilised at depth by low oxygen fugacity environments. Magnesium, iron, and other metallic compounds act as buffers throughout the process. The presence of reduced, elemental forms of carbon like graphite would indicate that carbon compounds are reduced as they descend into the mantle.
Polymorphism alters carbonate compounds’ stability at different depths within the Earth. To illustrate, laboratory simulations and density functional theory calculations suggest that tetrahedrally coordinated carbonates are most stable at depths approaching the core–mantle boundary. A 2015 study indicates that the lower mantle’s high pressure causes carbon bonds to transition from sp2 to sp3 hybridised orbitals, resulting in carbon tetrahedrally bonding to oxygen. CO3 trigonal groups cannot form polymerisable networks, while tetrahedral CO4 can, signifying an increase in carbon’s coordination number, and therefore drastic changes in carbonate compounds’ properties in the lower mantle. As an example, preliminary theoretical studies suggest that high pressure causes carbonate melt viscosity to increase; the melts’ lower mobility as a result of its increased viscosity causes large deposits of carbon deep into the mantle.

Accordingly, carbon can remain in the lower mantle for long periods of time, but large concentrations of carbon frequently find their way back to the lithosphere. This process, called carbon outgassing, is the result of carbonated mantle undergoing decompression melting, as well as mantle plumes carrying carbon compounds up towards the crust. Carbon is oxidised upon its ascent towards volcanic hotspots, where it is then released as CO2. This occurs so that the carbon atom matches the oxidation state of the basalts erupting in such areas.
Carbon in the core
Although the presence of carbon in the Earth’s core is well-constrained, recent studies suggest large inventories of carbon could be stored in this region. Shear (S) waves moving through the inner core travel at about fifty percent of the velocity expected for most iron-rich alloys. Because the core’s composition is believed to be an alloy of crystalline iron and a small amount of nickel, this seismic anomaly indicates the presence of light elements, including carbon, in the core. In fact, studies using diamond anvil cells to replicate the conditions in the Earth’s core indicate that iron carbide (Fe7C3) matches the inner core’s wave speed and density. Therefore, the iron carbide model could serve as an evidence that the core holds as much as 67% of the Earth’s carbon. Furthermore, another study found that in the pressure and temperature condition of the Earth’s inner core, carbon dissolved in iron and formed a stable phase with the same Fe7C3 composition—albeit with a different structure from the one previously mentioned. In summary, although the amount of carbon potentially stored in the Earth’s core is not known, recent studies indicate that the presence of iron carbides can explain some of the geophysical observations.
Human influence


Since the industrial revolution, human activity has modified the carbon cycle by changing its components’ functions and directly adding carbon to the atmosphere.
The largest human impact on the carbon cycle is through direct emissions from burning fossil fuels, which transfers carbon from the geosphere into the atmosphere. The rest of this increase is caused mostly by changes in land-use, particularly deforestation.
Another direct human impact on the carbon cycle is the chemical process of calcination of limestone for clinker production, which releases CO2. Clinker is an industrial precursor of cement.
Humans also influence the carbon cycle indirectly by changing the terrestrial and oceanic biosphere. Over the past several centuries, direct and indirect human-caused land use and land cover change (LUCC) has led to the loss of biodiversity, which lowers ecosystems’ resilience to environmental stresses and decreases their ability to remove carbon from the atmosphere. More directly, it often leads to the release of carbon from terrestrial ecosystems into the atmosphere. Deforestation for agricultural purposes removes forests, which hold large amounts of carbon, and replaces them, generally with agricultural or urban areas. Both of these replacement land cover types store comparatively small amounts of carbon so that the net product of the process is that more carbon stays in the atmosphere.
Other human-caused changes to the environment change ecosystems’ productivity and their ability to remove carbon from the atmosphere. Air pollution, for example, damages plants and soils, while many agricultural and land use practices lead to higher erosion rates, washing carbon out of soils and decreasing plant productivity.
Humans also affect the oceanic carbon cycle. Current trends in climate change lead to higher ocean temperatures, thus modifying ecosystems.Also, acid rain and polluted runoff from agriculture and industry change the ocean’s chemical composition. Such changes can have dramatic effects on highly sensitive ecosystems such as coral reefs, thus limiting the ocean’s ability to absorb carbon from the atmosphere on a regional scale and reducing oceanic biodiversity globally.
Arctic methane emissions indirectly caused by anthropogenic global warming also affect the carbon cycle and contribute to further warming in what is known as climate change feedback.
On 12 November 2015, NASA scientists reported that carbon dioxide in the atmosphere from human sources continues to increase, reaching levels not seen in hundreds of thousands of years. Currently, the rate of carbon dioxide released by the burning of fossil fuels is about double the net uptake by vegetation and the ocean.
Cycle du carbone
Le cycle du carbone est le cycle biogéochimique (ensemble des échanges d’un élément chimique) du carbone sur une planète. Celui de la Terre est rendu plus complexe par l’existence d’importantes masses d’eau océaniques, et surtout par le fait que la vie (et donc les composés carbonés qui en sont le substrat) y tient une place importante. Il est caractérisé par l’importance relative des stocks emmagasinés dans les quatre grands réservoirs naturels de carbone de la planète (atmosphère, biosphère, hydrosphère et lithosphère), par les échanges entre ces réservoirs, et le renouvellement dynamique (appelé turnover) général du carbone du sol (pédosphère) qui inclut généralement la minéralisation (conversion du carbone organique en CO2) et la transformation d’un pool (ou réservoir) de carbone à un autre (matière organique du sol (en) fraîche et matière organique humifiée).
L’étude des cycles des principaux éléments chimiques (dont le carbone) a toujours été d’un grand intérêt scientifique et technique ; cela permet notamment d’évaluer la disponibilité, prédire les conditions et zones d’accumulation (pour une exploitation), définir les leviers à actionner pour optimiser localement une production sensible à un élément, etc. Le cycle du carbone est très important pour la biosphère, puisque la vie est fondée sur l’utilisation de composés à base de carbone : la disponibilité en carbone fait partie des facteurs primordiaux pour le développement des êtres vivants sur Terre.
Enfin l’étude de ce cycle a récemment pris un relief tout particulier dans le cadre de la question du réchauffement climatique : deux des gaz à effet de serre en cause, le dioxyde de carbone (CO2) et le méthane (CH4), participent au cycle du carbone, dont ils sont la principale forme atmosphérique. Plus largement que les questions climatiques, l’étude du cycle du carbone permettra de déterminer les effets du relargage par les activités humaines du carbone stocké sous forme de combustibles fossiles.

Réservoirs de carbone et vitesses d’échanges

Il existe quatre types de réservoirs de carbone :
- l’atmosphère et l’hydrosphère (océans principalement), où le carbone est diffus et dissout principalement sous forme de gaz carbonique (CO2), et plus marginalement de méthane (CH4) ;
- la biosphère, où le carbone est fixé dans la biomasse, sous forme de carbone organique ou de constituant squelettique (y compris en mer, sous forme de biomasse planctonique) ;
- la lithosphère, où le carbone est fixé sous forme de roches fossiles, combustible (pétrole, charbon, gaz) ou calcaire ;
- le manteau terrestre, où du gaz carbonique est présent sous forme diffuse et dissoute.
Le cycle naturel du carbone dans le système Terre peut être évalué en analysant la dimension, les flux d’échanges et le temps de résidence d’un atome de carbone dans les différents réservoirs.
En termes de flux, l’essentiel du cycle se fait entre l’atmosphère, les couches superficielles du sol et des océans, et la biosphère (biomasse et nécromasse). Sur les continents, les tourbières, prairies et forêts, mais aussi certains sols jouent un rôle plus ou moins important de stockage intermédiaire de carbone, ou de puits de carbone. Les échanges de carbone se mesurent en milliards de tonnes (gigatonnes) par an (Gt/an). Le principal flux est celui entre biosphère et atmosphère, de l’ordre de 60 Gt an−1, correspondant d’un côté à la photosynthèse, et de l’autre à la respiration et la décomposition aérobies. Les flux géologiques sont de deux ordres de grandeur plus faibles, avec le dégazage de CO2 par le volcanisme (0,1 Gt an−1), la fossilisation de roches combustibles (0,1 Gt an−1), et la sédimentation de roches carbonatées (0,3 Gt an−1).
En termes de masses, la plus grande partie du carbone terrestre est piégée dans la lithosphère, sous forme de composés qui participent peu au cycle : roches sous forme de carbonates et combustibles fossiles. Par ordre de taille décroissante, on distingue :
- un immense réservoir (> à 50 millions de Gt de carbone) qui correspond aux sédiments et roches sédimentaires présentes dans la lithosphère, ainsi que le manteau terrestre ;
- un réservoir de taille moyenne (39 000 Gt de carbone) constitué par les masses d’eaux océaniques superficielles et profondes ;
- et plusieurs réservoirs de petite taille, c’est-à-dire inférieurs à 2 000 Gt de carbone comprenant : l’atmosphère (800 Gt de carbone), la biosphère (organismes vivants, 600 Gt de carbone) et le sol (1500 Gt de carbone à 1 m de profondeur).
Cycle géologique du carbone
Cycle carbonate-silicate
99,6 % du carbone terrestre (correspondant à approximativement 108 gigatonnes de carbone) est piégé dans le réservoir géologique, et évolue à des vitesses géologiques. Pour l’essentiel, tout le carbone est passé à un moment ou à un autre de son histoire sous forme de carbonate. Par contraste, la biosphère ne concerne que 0,002 % du carbone terrestre.
Le cycle du carbone débute par l’arrivée du dioxyde de carbone (CO2) à la surface de la Terre. Elle résulte du dégazage du manteau terrestre lors des éruptions volcaniques, qui rejettent dans l’atmosphère divers gaz dont le CO2 et le monoxyde de carbone (CO). Ainsi, l’atmosphère primitive de la Terre était principalement composée de CO2. Aujourd’hui, ce dégazage continue selon un flux faible, soit environ 0,1 Gt/an.
Au cours des âges, et alors que la température du soleil augmente, la plupart de ce CO2 originel a été peu à peu piégée surtout par des processus biologiques dans des « réservoirs » tels que la lithosphère (roches carbonatées, charbon…), la biosphère ou les océans.
Cycle chimique
Les interactions chimiques du CO2 avec la lithosphère et l’hydrosphère ont été décrites par Harold Clayton Urey en 1952, mais avaient déjà été étudiées par Jacques-Joseph Ebelmen dès 1845.
Le gaz carbonique présent dans l’atmosphère se dissout dans l’eau pour former de l’acide carbonique, présent dans les eaux de pluie et de ruissellement : CO2 + H2O ↔ H+ + HCO3−
L’acide carbonique est un acide faible, mais au fil des temps géologiques il contribue à l’érosion en rongeant les silicates, par exemple de la wollastonite de formule CaSiO3 (ainsi bien entendu que les carbonates), les dissociant en silice et en ions calcium, qui restent dissous :
CaSiO3 + 2 H+ → Ca2+ + SiO2 + H2O
À ce stade, le gaz carbonique est consommé pour produire de la silice et du bicarbonate en solution, par lequel il est fixé :
CaSiO3 + 2 CO2 + H2O → Ca2+ + 2 HCO3− + SiO2
Lorsqu’il précipite naturellement, le bicarbonate se transforme en carbonate. Dans le cycle biologique, les organismes aquatiques et surtout marins utilisent ces ions calcium pour bâtir leur squelette et coquilles, ce qui après leur décès sédimente et réalise une précipitation biologique de carbonate, pratiquement insoluble : Ca2+ + CO3H– → CaCO3↓ + H+
En pratique, l’équation est équilibrée sur le plan ionique par un deuxième ion bicarbonate, et la précipitation du carbonate s’accompagne de la restitution de CO2 : Ca2+ + 2 CO3H– → CaCO3↓ + CO2 ↑ +H2O
Au bilan, la transformation en milieu aqueux du silicate en silice et carbonate fixe une mole de gaz carbonique :
CO2 + CaSiO3 → SiO2 + CaCO3
Après avoir sédimenté sur les fonds marins, où ils deviennent piégés, les carbonates peuvent avoir deux destins possibles suivant le devenir de leur couche géologique. À la suite de mouvements tectoniques, un bassin sédimentaire peut se trouver soulevé et exposé par l’orogenèse, ce qui l’expose à l’érosion et réalise l’inverse de la précipitation biologique : CaCO3 + H+ → Ca2+ + HCO3−
Alternativement, la plaque océanique chargée de carbonates peut disparaître dans le manteau terrestre, à travers une fosse de subduction. Dans ces conditions de température et de pression élevées, le carbonate réagit avec la silice présente pour former de nouveaux silicates et du gaz carbonique : CaCO3 + SiO2 → CaSiO3 + CO2
Le gaz carbonique du manteau peut ensuite s’échapper avec les éruptions volcaniques, bouclant le cycle.
Rétroactions
Le cycle entraîne une rétroaction négative critique entre les niveaux de dioxyde de carbone et les changements climatiques. Si par exemple le CO2 s’accumule dans l’atmosphère, l’effet de serre augmentera la température de surface, ce qui augmentera également le taux de précipitations et l’altération du silicate, ce qui éliminera le carbone de l’atmosphère. De ce fait, le cycle carbonate-silicate a un effet stabilisateur sur le climat de la Terre sur de longues périodes, raison pour laquelle il a été appelé « le thermostat de la Terre ».
À l’échelle de dizaines, voire de centaines de millions d’années, les niveaux de dioxyde de carbone dans l’atmosphère peuvent varier en raison de perturbations naturelles du cycle. Des modifications de la surface de la planète, telles que l’absence de volcans ou l’élévation du niveau de la mer, qui réduiraient la quantité de surface exposée aux intempéries, peuvent modifier les vitesses auxquelles se déroulent les différents processus de ce cycle.
Intérêt du volcanisme et de ses dégagements du CO2 dans l’histoire de la Terre
À plusieurs périodes dans l’histoire de la Terre, celle-ci a connu des refroidissements tels qu’elle était entièrement recouverte de glace des pôles à l’équateur. C’est la théorie de la « Terre boule de neige » (Snowball Earth). Un de ces événements eut lieu au Paléo protérozoïque (2,2 à 2,3 milliards d’années), et 3 ou 4 autres glaciations totales se seraient déroulées au Néoprotérozoïque (entre 730 à 590 millions d’années). Ce phénomène peut être expliqué par l’augmentation de la pluie, le ruissellement et donc l’érosion de surface, et la présence de multiples autres facteurs qui vont conduire à la chute du taux de CO2 atmosphérique.
Les volcans auraient joué un grand rôle en mettant fin à la glaciation « boule de neige ». Malgré la présence de glace partout, les éruptions volcaniques ont perduré et ont permis d’augmenter le taux de CO2 dans l’atmosphère qui a induit un réchauffement. C’est grâce à des cataclysmes volcaniques que notre planète a pu sortir de son état de sphère gelée. La présence du CO2 fut à l’origine de l’explosion de la vie, en permettant de ramener la température de la Terre dans une plage idéale (15 °C de moyenne) où les organismes vivants peuvent se développer.
L’ensemble volcans et monde vivant, plus précisément le plancton des océans, a permis d’ajuster le taux de CO2 de l’atmosphère terrestre. En effet, les volcans rejettent des quantités gigantesques de dioxyde de carbone dans l’atmosphère et favorisent l’explosion de la vie. Le plancton lui est venu tamponner cet effet en absorbant une partie du CO2 relargué et s’en sert encore aujourd’hui pour former sa coquille (formée souvent de CaCO3), éliminant ainsi une grande partie du dioxyde de carbone.
Circulation océanique et atmosphérique
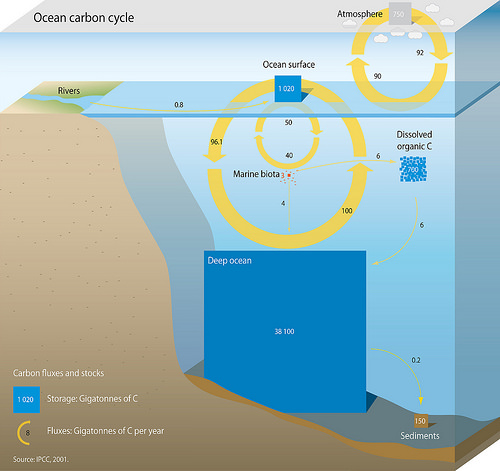
Répartition entre atmosphère et hydrosphère

Le carbone « libre » sous forme de CO2 se répartit entre l’atmosphère et l’hydrosphère, ces deux réservoirs étant en échanges constants.
Conceptuellement, l’océan peut être divisé en une couche de surface, de quelques centaines de mètres ou moins, dans laquelle l’eau établit un contact fréquent (quotidien ou annuel) avec l’atmosphère, et une couche profonde en dessous de la couche mélangée, dans laquelle le temps entre les contacts consécutifs peut être des siècles.
Le carbone inorganique dissout dans la couche de surface est échangé rapidement avec l’atmosphère, en maintenant l’équilibre. Le sens de ces échanges dépend de la latitude, car la solubilité du CO2 dépend de la température de l’eau des océans (les eaux froides contiennent plus de gaz dissous que les eaux chaudes). En se réchauffant, les masses d’eau océaniques tendent à dégazer leur CO2 dissout ; et quand elles migrent vers les zones polaires, ces masses d’eau se chargent au contraire en CO2 atmosphérique. Arrivées aux zones polaires, les masses d’eau, refroidies jusqu’à leur maximum de densité, plongent en entraînant le CO2 dissout. dans les couches profondes océaniques.
Les échanges se font essentiellement au niveau de la couche supérieure océanique, brassée par les vents et courants. La vitesse des échanges dépend de l’état de l’interface air-eau, donc du vent et de la hauteur de la houle : plus la surface de l’eau sera agitée et plus les échanges seront facilités… Les couches profondes océaniques sont sensiblement isothermes, au maximum de densité de l’eau, et ne font pas l’objet de dégazages ou d’absorption significatifs au cours de leur circulation. Ce n’est qu’après qu’un upwelling les ait remises en surface qu’elles peuvent se réchauffer et dégazer leur CO2, après une circulation thermohaline de l’ordre de 1 500 ans.
Principalement en raison de son volume plus important, et en partie parce que sa concentration en éléments gazeux carbonés est environ 15% plus élevée que la moyenne des eaux de surface, l’océan profond contient beaucoup plus de carbone – c’est le plus grand bassin de carbone à cycle actif dans le monde, contenant 50 fois plus que l’atmosphère. Mais le temps nécessaire pour atteindre l’équilibre avec l’atmosphère se compte ici en centaines d’années: l’échange de carbone entre les deux réservoirs océaniques est lent à échelle humaine.
Equilibres chimiques
Du fait de la forte solubilité du dioxyde de carbone (CO2) dans l’eau, et de l’importance du volume des océans, la capacité de stockage de l’hydrosphère est impressionnante : 63 fois plus élevée que celle de l’atmosphère.
Le carbone s’y retrouve sous diverses formes. En milieu aqueux, le CO2 est en équilibre avec les formes hydrogénocarbonate (HCO3−) et ion carbonate (CO32−) : CO2 + H2O ↔ HCO3− + H+ ↔ CO32− + 2 H+
La répartition de CO2 dans l’océan est approximativement la suivante : 1 % dans le dioxyde de carbone (CO2) ; 90 % dans l’hydrogénocarbonate (HCO3−) ; 9 % dans les ions carbonates (CO32−).
Ces proportions dépendent du pH de l’eau et par conséquent sont très variables dans les eaux continentales.
Cet acide tend à attaquer les carbonates présents dans les fonds océaniques, libérant du CO2 : CaCO3 + 2 H+ → Ca2+ + CO2 + H2O
Globalement, l’arrivée de CO2 sur le carbonate de calcium conduit à la formation de bicarbonate de calcium :
CaCO3 +CO2 + H2O → Ca2+ + 2 HCO3−
Cette réaction limite la présence de l’ion hydrogène au profit du calcium dissout, et rend les océans plutôt basiques à cause du bicarbonate. Inversement, une arrivée massive de CO2 peut dépasser la capacité tampon des carbonates, et provoquer une acidification des océans.
Rétroaction climatique

La réaction du cycle atmosphérique du carbone à des variations de température est plutôt complexe.
À court terme, une élévation de la température moyenne des océans diminue la capacité des eaux de surface à capturer le CO2. Toutes choses égales par ailleurs, le CO2 va dégazer dans l’atmosphère, augmentant la teneur atmosphérique moyenne. Cette augmentation conduit à un effet de serre, qui tend à accentuer la hausse de température et donc le dégazage. Cependant, le volume de la couche océanique superficielle reste limité, et à court terme, cet effet est freiné par le développement de la biosphère, en particulier du plancton marin, qui fixe une partie du carbone sous forme de carbone biologique, et en fait précipiter une autre partie sous forme de carbonates et de déchets organiques.
À plus long terme, la circulation thermohaline fait plonger les eaux les plus denses ; et donc le fond des océans reste à une température sensiblement constante, celle du maximum de densité, tant qu’il reste des régions polaires où ces températures puissent être atteintes. En présence d’une atmosphère plus chargée en CO2, ces eaux froides seront elles-mêmes plus chargées lors de leur plongeon, et augmenteront de ce fait la masse de CO2 présente dans ce réservoir des eaux océaniques profondes.
Les variations de la pression partielle du CO2 dans l’air modifie les flux entre l’atmosphère et les eaux. Étant donné les valeurs très élevées des flux d’échanges dans les deux sens, une augmentation de teneur en CO2 atmosphérique (réservoir de 800 Gt) de 2 à 3 % correspond à une arrivée dans l’océan d’environ 2 à 3 Gt de carbone par an.
La quantité de CO2 dissoute dans l’océan varie avec son pH, du fait de l’équilibre de dissociation : CO2↑ + H2O ↔ H+ + HCO3−
Dans un milieu plus acide, si le pH diminue d’une unité (augmentation du H+ présent), le pCO2 augmente d’un facteur dix. De même, si l’océan devient plus chargé en gaz carbonique, l’équilibre est déplacé vers la droite et il s’acidifie.
Cycle du carbone biologique
Échanges atmosphère-biosphère
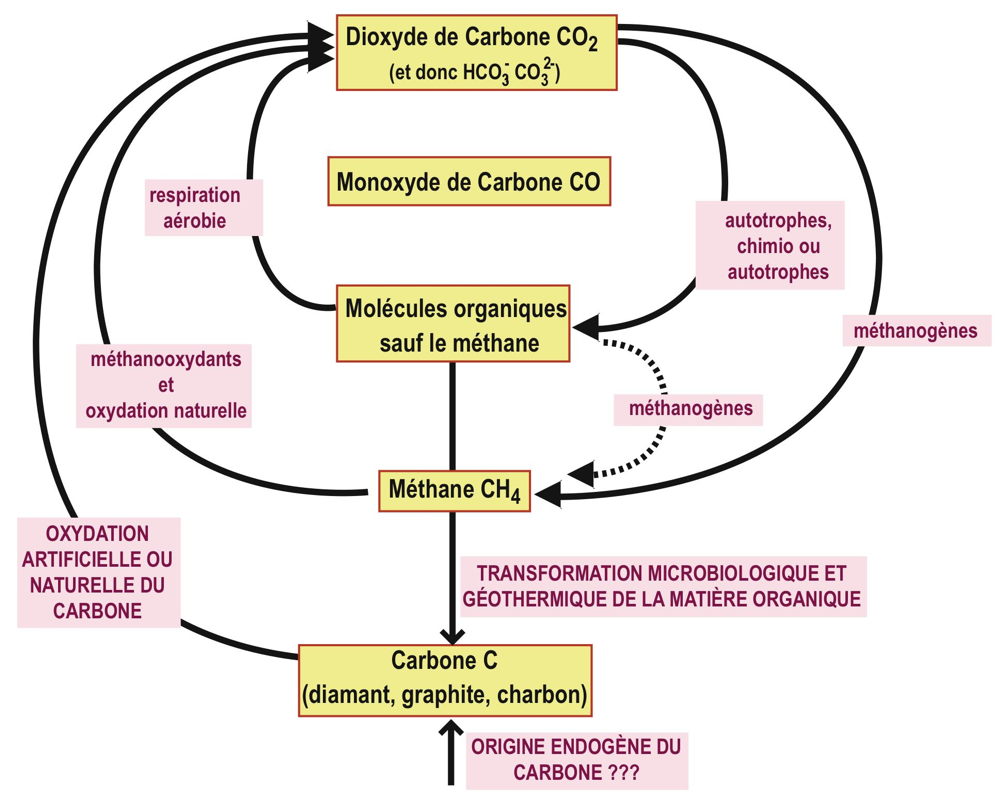
Les êtres vivants échangent 60 Gt/an de carbone avec l’atmosphère. Cet échange se fait dans les deux sens : alors que la fermentation, la respiration des bactéries, des animaux et des végétaux dégagent du CO2, la photosynthèse (notamment celle des végétaux chlorophylliens) fixe le carbone dans la matière organique ou biomasse. Ces deux mécanismes font à la fois partie du cycle du carbone et du cycle de l’oxygène. La photosynthèse produit essentiellement un hydrate de carbone, dont la formule brute superpose du carbone et de l’eau, et de l’oxygène, à partir d’eau et de gaz carbonique. On aura par exemple, pour la fabrication du glucose : 6 CO2 + 6 H2O → C6H12O6 + 6 O2
Inversement, la respiration consomme ces matières organiques et de l’oxygène pour produire du gaz carbonique et de l’eau, ce qui correspond globalement à une oxydation de la matière organique.
Dans un écosystème en équilibre, à biomasse constante, la quantité nette de dioxygène produit par les organismes autotrophes (photosynthèse) est égale à la quantité de dioxygène consommée par les organismes hétérotrophes (respiration). Ceci suppose que toute la matière organique sert effectivement à de la respiration, donc ne sort pas de la biosphère mais est consommée par son producteur, des prédateurs, des nécrophages, ou des micro-organismes fossoyeurs.
Mais les écosystèmes ne sont en général pas équilibrés. Globalement, un peu de matière organique s’échappe de la biosphère et n’est pas oxydée, et contribue alors à un stockage de carbone, par la sédimentation, la fossilisation, la formation de kérogène, etc. (voir infra biosphère-lithosphère). Les tourbières par exemple stockent des débris végétaux dans les sols, la tourbe. Cette biomasse « morte » est estimée à 1 600 Gt de carbone, deux fois la quantité de carbone de la biomasse « vivante ». C’est pourquoi le stockage de carbone dans les sols est considéré comme une potentielle solution pour atténuer les émissions de dioxyde de carbone dans l’atmosphère (e.g. 4p1000).
Les ions carbonates seront eux-mêmes en équilibre avec des formes précipitées (carbonate de calcium, qu’on retrouve notamment dans les coquilles d’animaux marins qui formeront le calcaire).
Enfin, le développement des êtres vivants qui captent le CO2 (photosynthèse, construction d’une coquille) ou en rejettent (respiration) a une importance non négligeable sur la quantité de carbone dissous et représente une part de la biomasse.
Rôle des forêts, anciennes notamment
Pendant sa phase de croissance initiale une forêt joue un rôle de puits de carbone : la masse de carbone sous forme de branches, racines et humus augmente à partir de zéro. Par contre, il n’y a pas de consensus scientifique concernant les forêts anciennes.
Une hypothèse posée par Eugène Odum dans les années 1960 était que ces forêts étaient à l’état d’équilibre, c’est-à-dire émettant autant de CO2 qu’elles en absorbent, parce qu’elles ne transféreraient pas de matériaux organiques dans les sols profonds et finalement les couches géologiques. Contrairement aux tourbières, les vastes zones forestières auraient alors été neutres dans le cycle du carbone.
Une étude internationale récente infirme cette hypothèse, montrant que globalement, comme les jeunes forêts, les forêts anciennes peuvent stocker aussi du carbone (plus ou moins selon le contexte climatique et les apports atmosphériques en azote, mais tout à fait significativement). Les auteurs de cette étude invitent donc à intégrer dans les bilans les forêts de 15 et 800 ans d’âge, et surtout à mieux les protéger car leur destruction ou même leur perturbation est cause d’importants relargages de carbone. En effet, les données récentes des réseaux d’observatoires « CarboEurope » et « AmeriFlux » ont prouvé que ces forêts anciennes séquestrent annuellement de 0,8 à 1,8 milliard de tonnes de carbone. Les forêts anciennes comptent encore pour environ 15 % de la surface forestière totale (forêt primaires pour 30 % de cette surface, dont la moitié est la forêt boréale située dans l’hémisphère Nord, couvrant (6 x 108 hectares). Elles n’étaient jusqu’ici pas prises en compte dans les bilans-carbone, alors qu’elles séquestrent selon cette étude, notamment dans les transferts vers les litières et leurs sols au moins 10 % de tout le CO2 stocké.
Échanges lents avec la lithosphère
Échanges biosphère-lithosphère (fossilisation)
La fossilisation des êtres vivants morts demande plusieurs millions d’années. Comme le nombre d’organismes vivants ne peut pas augmenter brutalement de manière significative, ce transfert ne change guère au cours du temps. Il est estimé à moins de 0,5 Gt/an.
Échanges hydrosphère-lithosphère (sédimentation)
La « sédimentation océanique » : les coquilles des crustacés, des mollusques ou des algues planctoniques se forment par précipitation du calcaire à partir des éléments dissous : Ca2+ + 2 HCO3− ↔ CaCO3 + CO2 + H2O.
Cette précipitation peut être spontanée dans certaines conditions physico-chimiques.
La sédimentation des coquilles est à l’origine de la plupart des roches contenant du calcaire (craie, calcaire, marne etc.). Ce calcaire ou carbonate de calcium (CaCO3) reste stocké pendant des centaines de millions d’années (délai de renouvellement moyen : 330 millions d’années, à comparer avec le délai de renouvellement du carbone de l’atmosphère qui est de cinq ans).
Conclusion des échanges
Le cycle du carbone est donc un système de recyclage (en) très complexe où les processus physiques, chimiques et biologiques sont si intimement liés qu’il devient difficile d’examiner séparément le recyclage des deux formes de carbone (carbone organique et inorganique).
Si le cycle du carbone semble équilibré sur l’échelle des temps géologiques, il arrive souvent que les quantités et les flux de carbone varient de façon assez importante entre différents réservoirs et ont ainsi des implications climatiques majeures.
Les activités humaines participent au cycle du carbone

Les quantités de carbone émis par les activités humaines dans l’atmosphère sont de :
- 6,4 Gt/an pour les années 1990 ;
- 7,2 Gt/an pour la période 2000-2005 ;
- 10 Gt/an pour 2000-2006 selon l’Académie nationale des sciences des États-Unis, soit 37 % de plus qu’en 1990.
Environ la moitié de ce carbone a été réabsorbée par la biosphère, par photosynthèse accrue, et les océans, par dissolution.
Ainsi, la quantité de carbone dans l’atmosphère s’est accrue de 3,2 à 3,3 Gt/an dans la période 1990-1999.
Combustion
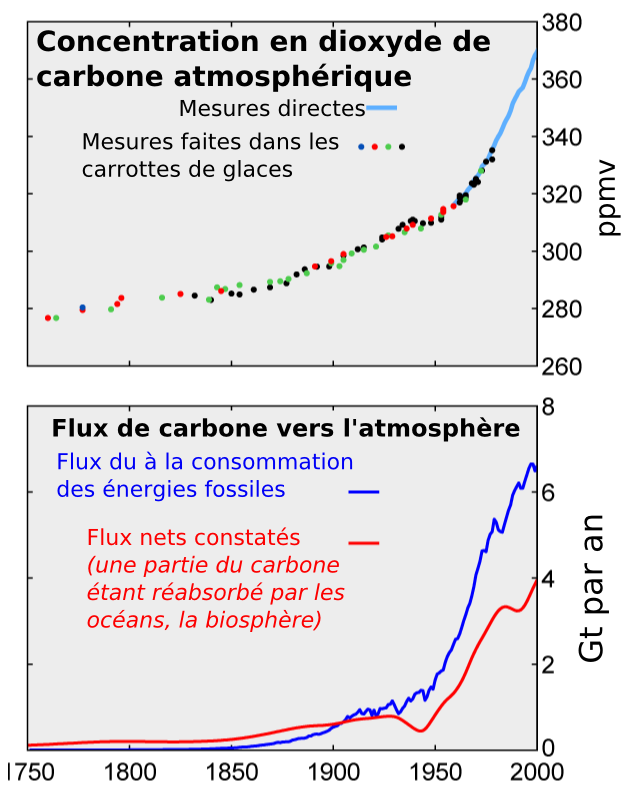
Les interventions les plus évidentes de l’homme sont :
- la combustion massive de matières organiques due à la déforestation,
- la combustion de roches carbonées (charbon, pétrole, gaz naturel) qui rejettent énormément de dioxyde de carbone et de méthane.
Fabrication du ciment
La fabrication du ciment se fait, entre autres processus, par la calcination du calcaire dans les fours à calcination, dans lesquels CaCO3 est converti en CaO (chaux) avec un rejet de CO2 dans l’atmosphère : CaCO3 minéral ou roche → CaO solide + CO2 gaz
Ce dégagement initial de CO2 lors de la calcination du calcaire ne parait pas très préoccupant. En effet, lors de l’utilisation du ciment produit, la réaction physico-chimique complexe de prise des mortiers & bétons absorbe du CO2 contenu dans l’air dans les mêmes proportions. Dans un premier temps, la transformation de chaux vive en chaux éteinte s’effectue par ajout d’eau (H2O). Cette opération d’extinction, conduite dans un hydrateur industriel, produit l’hydroxyde de calcium Ca(OH)2, avec un fort dégagement de chaleur : CaO + H2O → Ca(OH)2 + 1 155 kJ/kg
Dans un deuxième temps, la prise de la chaux dite « aérienne » s’effectue par carbonatation, c’est-à-dire en réabsorbant autant de dioxyde de carbone (CO2) présent dans l’atmosphère qu’il en avait été précédemment rejeté : Ca(OH)2 + CO2 → CaCO3 + H2O
En revanche, la calcination initiale nécessite beaucoup d’énergie, souvent d’origine fossile. C’est à cause de cette calcination que la fabrication du ciment est à l’origine d’environ 7 à 8 % des émissions totales de CO2 à l’échelle du globe.
La consommation d’énergie à partir de combustible fossile provoque un flux faible (0,2 Gt/an), quoique non négligeable ; le stockage du carbone dans les roches calcaires se ferait à une vitesse équivalente ou légèrement supérieure.
Effet du réchauffement climatique sur le cycle du carbone
Le cycle du carbone dépend du climat et réciproquement. Les interactions sont complexes, avec des phénomènes qui contribuent à une rétroaction positive, d’autres à une rétroaction négative. Tous les phénomènes ne sont pas complètement identifiés et quantifiés, mais on peut quand même en citer quelques-uns :
- Le CO2 et le méthane atmosphériques contribuent à l’effet de serre : une augmentation de leur taux est un facteur de réchauffement climatique
- Le réchauffement climatique diminue la dissolution du CO2 dans les océans : la solubilité du dioxyde de carbone dans les océans dépend de leur température. Si cette température augmente, la capacité de stockage inorganique des océans diminue et ils se mettent à rejeter eux-mêmes du dioxyde de carbone. L’enclenchement d’un tel cercle vicieux serait catastrophique.
- Le réchauffement climatique peut diminuer le transfert du CO2 vers les eaux profondes, et donc diminuer encore davantage sa dissolution dans les eaux superficielles. S’il prend trop d’ampleur, il pourrait aussi diminuer en grande partie la sédimentation océanique, en ralentissant, voire supprimant sous certaines latitudes, les courants océaniques profonds de la plongée (au niveau du Groenland pour le Gulf Stream et dans l’Océan Pacifique pour la branche asiatique) des eaux froides et plus salées chargée de dioxyde de carbone. Même si cette sédimentation est très faible, c’est elle qui génère l’ensemble des roches carbonatées, c’est-à-dire contenant des carbonates tels le carbonate de calcium (calcaire).
- Le réchauffement climatique augmente la dégradation de la matière organique des sols gelés (pergélisol) et des milieux tourbeux ce qui rejette du CO2 et du méthane, aggravant l’effet de serre additionnel.

