INTRODUCTION.
Les bilans matières sont à la base de la conception des procédés industriels. Un bilan matière repris sur l’ensemble du procédé déterminera les quantités de matières premières nécessaires et celles des produits fabriqués. Les balances sur les unités du procédé individuelles définissent les flux et les compositions du flux du procédé et fournissent les équations de base pour le dimensionnement des équipements.
Une bonne compréhension des calculs de bilan matière est essentielle dans la conception des procédés.
Dans ce chapitre, les principes fondamentaux du sujet sont abordés, en utilisant des exemples simples pour illustrer chaque concept. La pratique est nécessaire pour développer une expertise dans la gestion de ce qui peut souvent devenir ‘des calculs très complexes’. D’autres exemples et une discussion plus détaillée du sujet peuvent être trouvés dans les nombreux ouvrages spécialisés écrits sur les calculs des bilans matière et énergétique. Plusieurs textes appropriés sont répertoriés dans la section «Bibliographie» citée plus tard.
Pour les procédés complexes, les bilans matière sont généralement effectués à l’aide d’un logiciel de simulation de procédés (voir plus tard). Un temps et des efforts importants peuvent être gaspillés dans la simulation des procédés si les principes fondamentaux des bilans matière et énergétique ne sont pas correctement compris. Une attention particulière doit être portée à la sélection de la meilleure base et des meilleures limites pour les bilans matière et énergétiques; à la prévision des rendements; à la compréhension des schémas de recyclage, de purge et de contournement (bypass). Les calculs abrégés (à main levée), du type illustré dans ce texte, doivent toujours être utilisés pour vérifier les résultats de la simulation d’un procédé. Des calculs courts peuvent également être utilisés pour accélérer la convergence des simulations en fournissant de bonnes estimations initiales des flux de recyclage et de rattrapage (make-up stream en anglais, c’est quoi?). Les bilans matières sont également des outils utiles pour l’étude du fonctionnement des installations industrielles et leur dépannage. Ils peuvent être utilisés pour vérifier les performances par rapport à la conception, pour étendre les données souvent limitées disponibles à partir de l’instrumentation de l’usine, pour vérifier les étalonnages des instruments et pour localiser les sources de perte de matière. Les bilans matières sont essentiels pour obtenir des données de haute qualité des laboratoires ou des usines pilotes.
L’ÉQUIVALENCE ENTRE LA MASSE ET L’ÉNERGIE.
Einstein a montré que la masse et l’énergie sont équivalentes. L’énergie peut être convertie en masse et la masse en énergie. Elles sont liées par l’équation d’Einstein:
E = m.c ^ 2
où:
E: énergie, J,
m: masse, kg,
c: la vitesse de la lumière dans le vide, 3.10 ^ 8 m / s.
La perte de masse associée à la production d’énergie n’est significative que dans les réactions nucléaires. L’énergie et la matière sont toujours considérées comme conservées séparément dans les réactions chimiques.
CONSERVATION DE LA MASSE.
L’équation de conservation générale pour tout système de procédé peut être écrite comme suit:
Matière en sortie = Matière en entrée + Génération -Consommation – Accumulation
Pour un procédé qui fonctionne en régime permanent, le terme d’accumulation est égal à zéro. Sauf dans les procédés nucléaires, la masse n’est ni générée ni consommée; mais si une réaction chimique a lieu, une espèce chimique particulière pourra être formée ou consommée dans le processus.
Quand il n’y a pas de réaction chimique, le bilan en régime permanent se réduit à:
Matière en sortie = Matière entrante
Une équation de bilan peut être écrite pour chaque espèce identifiable séparément présente: éléments, composés ou radicaux; et pour la matière totale. Les bilans peuvent être écrits pour la masse ou pour le nombre de moles.
Exemple :
2000 kg d’une suspension à 5% d’hydroxyde de calcium dans l’eau doivent être préparés en diluant une suspension à 20%. Calculez les quantités requises. Les pourcentages sont en poids.
Solution:
Supposons que les quantités inconnues de la suspension à 20% et de l’eau soient X et Y, respectivement.
Bilan matière sur Ca(OH)2:
In Out
X . 20/100=2000 . 5/100 (a)
Bilan sur l’eau:
X. (100- 20)/100+ Y= 2000.(100- 5)/100 (b)
D’après l’équation (a), X = 500 kg.
La substitution dans l’équation (b) donne Y = 1500 kg
Vérifier le bilan matière sur la quantité totale:
X + Y = 2000
500 + 1500 = 2000. C’est correct.
2.4. UNITÉS UTILISÉES POUR EXPRIMER DES COMPOSITIONS.
Lorsqu’une composition est spécifiée en pourcentage, il est important d’indiquer clairement la base: poids, molaire ou volume.
Les abréviations w/w, wt% et % wt sont utilisées pour la masse (poids). La base du volume est généralement abrégée en vol%, LV% ou v/v.
Exemple:
L’acide chlorhydrique de qualité technique a une force de 28% w/w. Exprimez-le sous forme de fraction molaire.
Solution:
Base de calcul 100 kg d’acide 28% w/w.
Masse moléculaire: eau 18, HCl 36,5
Masse HCl = 100. 0,28 = 28 kg
Masse d’eau = 100. 0,72 = 72 kg
kmol HCl = 28 / 36,5 = 0,77
kmol eau = 72/18 = 4,00
Nombre total de moles = 4,77
fraction molaire HCl = 0,77 / 4,77 = 0,16
fraction molaire eau = 4,00 / 4,77 = 0,84
Vérifier le total 1,00
Dans les limites de la précision requise pour les calculs techniques, les fractions volumiques peuvent être considérées comme équivalentes aux fractions molaires pour les gaz, jusqu’à des pressions modérées (disons 25 bar).
Les quantités traces (trace quantities) sont souvent exprimées en parties par million (ppm). La base, le poids ou le volume, doit être indiquée, par exemple ppmw ou ppmv.
ppm = (quantité de composant / quantité totale) .10 ^ 6
Remarque: 1 ppm = 10 ^ -4 pour cent.
Les quantités minimes (minute quantities) sont parfois exprimées en parties par milliard (ppb). Cela fait référence à un milliard américain (10 ^ 9), pas à un milliard britannique (10 ^ 12).
STOICHIOMÉTRIE.
L’équation stœchiométrique d’une réaction chimique indique sans ambiguïté le nombre de molécules des réactifs et des produits qui sont mis en jeu , à partir desquels les quantités peuvent être calculées.
L’équation doit être équilibrée.
Avec des réactions simples, il est généralement possible d’équilibrer l’équation stœchiométrique par inspection ou par des calculs d’essais et d’erreurs. Si des difficultés sont rencontrées pour équilibrer des équations complexes, le problème peut toujours être résolu en écrivant un bilan équilibré pour chaque élément présent.
La procédure est illustrée dans l’exemple suivant:
Exemple:
Rédiger et équilibrer l’équation globale pour la fabrication de
chlorure de vinyle à partir d’éthylène, de chlore et d’oxygène.
Solution:
Méthode: Écrivez l’équation en utilisant des lettres pour le nombre inconnu de molécules de chaque réactif et produit. Faites un équilibre sur chaque élément. Résolvez l’ensemble d’équations résultantes.
A (C2H4) + B (Cl2) + C (O2) = D (C2H3Cl) + E (H2O)
Équilibre sur le carbone:
2A = 2D, A = D
sur l’hydrogène:
4A = 3D + 2E
en remplaçant D = A donne E = A / 2
sur le chlore
2B = D, donc B = A / 2
sur l’oxygène
2C = E, C = E / 2 = A / 4
en mettant A = 1, l’équation devient:
C2H4 + 1/2 Cl2 + 1/4 O2 = C2H3Cl + 1/2 H2O
multiplier par le plus grand dénominateur pour supprimer les fractions:
4C2H4 + 2Cl2 + O2 = 4C2H3Cl + 2H2O
CHOIX DE LA LIMITE DU SYSTÈME.
La loi de conservation s’applique à l’ensemble du procédé et à toute subdivision de ce dernier. La limite du système définit la partie du procédé considérée. Les flux entrant et sortant du système sont ceux qui traversent la frontière et doivent s’équilibrer avec les matières produites ou consommées à l’intérieur de la frontière.
Tout procédé peut être divisé de manière arbitraire pour faciliter les calculs du bilan matière. Le choix judicieux des limites du système peut souvent grandement simplifier ce qui serait autrement des calculs difficiles et tortueux.
Des règles simples et rapides peuvent être données sur la sélection des limites appropriées pour tous les types de problèmes de bilan matière. Le choix de la meilleure subdivision pour un procédé particulier est une question de jugement et dépend de la compréhension de la structure du problème, qui ne peut être acquise que par la pratique. Les règles générales suivantes servent de guide:
- Avec des procédés complexes, prenez d’abord la frontière autour du procédé tout entier; et si possible calculer les flux entrants et sortants. Matières premières entrantes, produits et sous-produits sortants.
- Sélectionnez les limites pour subdiviser le procédé en étapes simples et faites un bilan sur chaque étape séparément.
- Sélectionnez la limite autour de n’importe quelle étape afin de réduire au minimum le nombre de flux inconnus.
- Dans un premier temps, incluez tous les flux de recyclage dans les limites du système (voir plus en bas).
Exemple:
Le diagramme montre les principales étapes d’un procédé de production d’un polymère. À partir des données suivantes, calculez les débits pour un débit de production de 10 000 kg / h.
Sélectivité du réacteur pour le polymère 100%
polymérisation en suspension 20% en masse de monomère / eau
conversion 90% par passage
catalyseur 1 kg / 1000 kg de monomère
agent d’arrêt court 0,5 kg / 1000 kg de monomère n’ayant pas réagi
Eau de lavage du filtre env. 1 kg / 1 kg de polymère
Rendement de la colonne de récupération 98% (pourcentage récupéré)
Le sécheur alimenté à presque 5% d’eau, spécification du produit qui en sort: 0,5% H2O
Pertes de polymère dans le filtre et le sécheur près de 1%.

Solution:
Seuls les flux nécessaires pour illustrer le choix des limites du système et la méthode de calcul sont donnés dans la solution.
Base de calcul: 1 heure
Prenez la première limite du système autour du filtre et du séchoir.
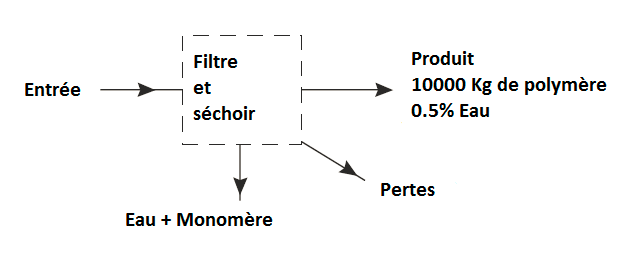
Avec 1% de perte, polymère entrant dans le sous-système
= 10 000 / 0,99
= 10101 kg
Prenez la deuxième frontière autour du système: réacteur; les alimentations du réacteur peuvent alors être calculées.
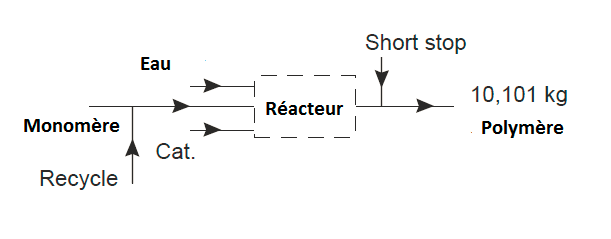
À 90% de conversion par passage, alimentation en monomère = 10101 / 0,9
= 11223 kg
Monomère n’ayant pas réagi = 11223 -10101 = 1122 kg
Short Stop, à 0,5 kg / 1000 kg de monomère n’ayant pas réagi = 1122. 0,5. 10 ^ -3 = 0,6 kg
Catalyseur, à 1 kg / 1000 kg de monomère = 11223. 1 . 10 ^ -3 = 11 kg
Mettons F1 l’eau d’alimentation du réacteur, puis pour 20% de monomère
0,2 = 11 223 / (F1 + 11 223)
F1 = 11 223. (1 -0,2) /0,2
= 44892 kg
Considérons maintenant à nouveau le sous-système filtre-sécheur.
Eau dans le polymère vers le sécheur, à 5% (en négligeant la perte de polymère)
= 10101. 0,05 / 0,95
= 532 kg
L’équilibre sur le sous-système réacteur-filtre-sécheur donne des débits à la colonne de récupération.
eau, 44892 +10101-532 = 54,461 kg
monomère, monomère n’ayant pas réagi = 1122 kg
Considérons maintenant le système de récupération:

Avec 98% de récupération, le recyclage vers le réacteur = 0,98. 1122 = 1100 kg
La composition de l’effluent est de 22 kg de monomère, 54461 kg d’eau.
Considérez l’alimentation en monomère du réacteur:

L’équilibre autour du T té donne le monomère frais requis
= 11223 – 1100 = 10123 kg
Notez que ce calcul en 12 lignes aurait nécessité la mise en place d’un recyclage et de trois ajustements de flux dans un simulateur de procédés, illustrant que des problèmes simples peuvent souvent être résolus plus facilement à la main ou à l’aide de calculs sur tableur si les limites des bilans de masse sont choisies avec soin.
CHOIX DE LA BASE DES CALCULS.
Le choix de la base d’un calcul détermine souvent si le calcul s’avèrera simple ou complexe. Comme pour le choix des limites du système, aucune règle ou procédure globale ne peut être donnée pour la sélection de la bonne base pour un problème. La sélection dépend du jugement acquis par l’expérience. Certaines règles guide sont:
A. Heure: Choisissez la base de temps dans laquelle les résultats doivent être présentés; par exemple kg/h, tonnes métriques/an, sauf si cela conduit à des nombres très grands ou très petits, où les erreurs d’arrondi peuvent devenir problématiques.
B. Pour les processus par lots (batch), utilisez un seul lot.
C. Choisissez comme base massique le débit pour lequel la plupart des informations sont données.
D. Il est souvent plus facile de travailler en moles plutôt qu’en masse, même en l’absence de réaction.
E. Pour les gaz, si les compositions sont données en volume, utiliser une base molaire, en se rappelant que les fractions volumiques sont équivalentes à des fractions molaires jusqu’à des pressions modérées.
NOMBRE DES ESPÈCES INDÉPENDANTS.
Une équation de bilan peut être écrite pour chaque espèce indépendante. Toutes les espèces d’un bilan matière ne seront pas toujours indépendantes.
Systèmes physiques, aucune réaction:
S’il n’y a pas de réaction chimique, le nombre des espèces indépendantes est égal au nombre d’espèces chimiques distinctes présentes.
Envisagez la production d’un acide de nitration en mélangeant 70% d’acide nitrique et 98% d’acide sulfurique. Le nombre d’espèces chimiques distinctes est de trois: l’eau, l’acide sulfurique, l’acide nitrique.

Systèmes chimiques, réaction:
Si le processus implique une réaction chimique, le nombre de composants indépendants n’est pas nécessairement égal au nombre d’espèces chimiques, car certaines peuvent être liées par des équations chimiques. Dans cette situation, le nombre de composants indépendants peut être calculé par la relation suivante:
Nombre de composants indépendants = Nombre d’espèces chimiques – Nombre d’équations chimiques indépendantes
Exemple:
Si l’acide de nitration est constitué en utilisant de l’oléum à la place de l’acide sulfurique à 98%, il y aura quatre espèces chimiques distinctes: l’acide sulfurique, le trioxyde de soufre, l’acide nitrique, l’eau. Le trioxyde de soufre réagira avec l’eau produisant de l’acide sulfurique, il n’y a donc que trois composants indépendants.
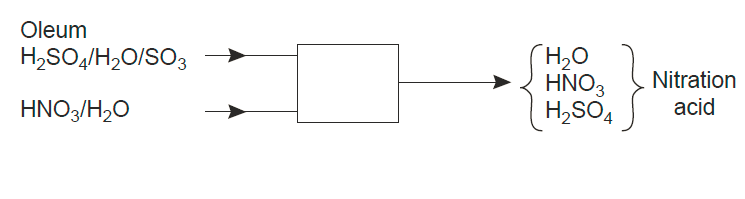
Solution:
Équation de réaction SO3 + H2O = H2SO4
Nombre d’espèces chimiques 4
Nombre de réactions 1
Nombre d’espèces indépendantes 4-1 = 3.
CONTRAINTES SUR LES FLUX ET LES COMPOSITIONS.
Il est évident, mais mérite d’être souligné, que la somme des flux de composants individuels dans un flux ne peut pas dépasser la quantité totale de ce dernier. De plus, la somme des fractions molaires ou massiques individuelles doit être égale à 1.
Par conséquent, la composition d’un flux est complètement définie si toutes les concentrations de composants sauf une sont données.
Les flux de composants dans un flux (ou les quantités dans un lot (ou batch)) sont complètement définis par l’un des éléments suivants:
A. Spécifier le débit (ou la quantité) de chaque composant.
B. Spécifier le débit total (ou la quantité) et la composition.
C. Spécifier le débit (ou la quantité) d’un composant et la composition.
Exemple:
Le courant d’alimentation d’un réacteur contient 16% d’éthylène, 9% d’oxygène, 31% d’azote et du chlorure d’hydrogène. Si le débit d’éthylène est de 5000 kg/h, calculez les débits des composants individuels et le débit total du flux. Tous les pourcentages sont en masse.
Solution
Pourcentage d’HCl = 100 – (16 + 9 + 31) = 44
Pourcentage d’éthylène = (5000 / total). 100 = 16
d’où le débit total = 5000. (100/16) = 31250 kg / h
donc, débit d’oxygène = (9/100). 31250 = 2813 kg / h
azote = 31250. (31/100) = 9687 kg / h
chlorure d’hydrogène = 31250. (44/100) = 13750 kg / h
Règle générale: Le rapport entre le débit de tout composant et le débit de tout autre composant est le même que le rapport des compositions des deux composants.
Le débit de tout composant dans cet exemple aurait pu être calculé directement à partir du rapport du pourcentage à celui de l’éthylène et du débit d’éthylène.
Flux de chlorure d’hydrogène = (44/16). 5000 = 13,750 kg / h
MÉTHODE ALGÉBRIQUE GÉNÉRALE.
Des problèmes simples de bilan matière impliquant seulement quelques flux et avec quelques inconnues peuvent généralement être résolues par des méthodes simples et directes. La relation entre les quantités inconnues et les informations données peut généralement être clairement vue. Pour des problèmes plus complexes, et pour des problèmes avec plusieurs étapes de traitement, une approche algébrique plus formelle peut être utilisée. La procédure est fastidieuse si les calculs doivent être effectués manuellement, mais doit aboutir à une solution même aux problèmes les plus insolubles, en fournissant des informations suffisantes pour que le problème ait une solution.
Des symboles algébriques sont attribués à tous les flux et compositions inconnus. Des équations de bilan de masse sont ensuite écrites autour de chaque sous-système pour les composants indépendants (espèces ou éléments chimiques).
Les problèmes de bilans matière sont des exemples particuliers du problème général de la conception des procédés discuté dans la page (process design, conception des procédés). Les inconnues sont des compositions ou des débits, et les équations associées découlent de la loi de conservation et de la stœchiométrie des réactions. Pour qu’un problème ait une solution unique, il doit être possible d’écrire le même nombre d’équations indépendantes qu’il y a d’inconnues.
Considérons le problème général du bilan matière où il y a Ns flux contenant chacun Nc composants indépendants. Ensuite, le nombre de variables, Nv, est donné par:
Nv = Nc. Ns
Si des équations d’équilibre indépendantes Ne peuvent être écrites, alors le nombre de variables, Nd, qui doivent être spécifiées pour une solution unique, est donné par:
Nd = (Ns. Nc) – Ne
Considérez un problème de mélange simple:
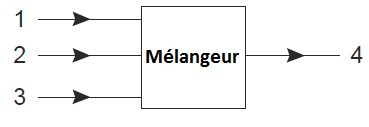
Soit Fn le débit total dans le flux n, et xn,m la concentration du composant m dans le flux n. Ensuite, l’équation du bilan générale peut être écrite:
F1.x1,m + F2.x2,m + F3.x3,m = F4.x4,m
Une équation de bilan peut également être écrite pour le total de chaque flux:
F1 + F2 + F3 = F4
mais cela pourrait être obtenu en ajoutant les équations des composants individuels, et il ne s’agit donc pas d’une équation indépendante supplémentaire. Il existe m équations indépendantes, le nombre de composantes indépendantes.
Ce problème a 4m variables et m équations d’équilibre indépendantes. Il y aura une solution unique au problème si nous spécifions 3m variables, par exemple, les débits molaires de tous les m composants dans les trois flux ou dans deux flux et le produit.
Considérons une unité de séparation, telle qu’une colonne de distillation, qui divise un flux en deux flux produits. Soit le débit d’alimentation: 10 000 kg / h; composition benzène 60%, toluène 30%, xylènes 10%.

Il existe trois flux (alimentation, distillat et Résidu) et trois composants indépendants dans chaque flux.
Nombre de variables (débits des 3 composants) = 9
Nombre d’équations indépendantes de bilan matières = 3
Nombre de variables à spécifier pour une solution unique = 9-3 = 6
Trois variables sont spécifiées; le débit et la composition de la charge fixent le flux de chaque composant dans la charge (l’alimentation).
Nombre de variables à spécifier par le concepteur = 6 – 3 = 3. Trois flux de composants peuvent être choisis.
Normalement, la composition et le débit supérieurs ou la composition et le débit inférieurs seraient choisis.
Si la fonction principale de la colonne est de séparer le benzène des autres composants, le maximum de toluène et de xylènes dans le distillat serait spécifié (par exemple, à 5 kg/h et 3 kg/h) et la perte de benzène dans le résidu également spécifiée (par exemple, à moins que 5 kg / h).
Trois débits sont spécifiés, les autres débits peuvent donc être calculés:
Benzène dans le distillat = benzène dans l’alimentation -benzène dans le résidu:
0.6. 10000 – 5 = 5995 kg / h
Toluène dans le résidu = toluène dans l’alimentation – toluène dans le distillat:
0,3. 10000 – 5 = 2995 kg / h
Xylènes dans le résidu = xylènes dans l’alimentation – xylènes dans le distillat:
0,1. 10000 – 3 = 997 kg / h
COMPOSANT DE NŒUD. (ou de liaison)
Dans ce qui précède, il a été montré que le débit de tout composant était dans le même rapport au débit de tout autre composant que le rapport des concentrations des deux composants. Si un composant passe inchangé dans une unité de traitement, il peut être utilisé pour lier les compositions d’entrée et de sortie.
Cette technique est particulièrement utile dans le traitement des calculs de combustion où l’azote dans l’air de combustion passe à travers sans réagir et est utilisé comme composant de nœud (ou de liaison). Ceci est illustré dans un exemple qui suit.
Ce principe est également souvent utilisé dans les expériences pour mesurer le débit d’un flux de procédé en introduisant un flux mesuré d’un matériau facilement analysé, compatible et inerte.
Exemple
Le dioxyde de carbone est ajouté à un débit de 10 kg / h à un courant d’air et l’air est prélevé à une distance suffisante en aval pour assurer un mélange complet. Si l’analyse montre 0,45% v/v CO2, calculez le débit d’air.
Solution:
La teneur normale en dioxyde de carbone de l’air est de 0,03%.

Base: kmol / h, en pourcentages en volume.
kmol / h CO2 introduit = 10/44 = 0,2273
Soit X le flux d’air.
Équilibre sur le CO2, le composant du lien
CO2 en = 0,0003X + 0,2273
CO2 sortant = 0,0045X
X (0,0045 – 0,0003) = 0,2273
X = 0,2273 / 0,0042 = 54 kmol / h
= 54. 29 = 1560 kg / h
Exemple
Dans un essai sur un four alimenté au gaz naturel (composition 95% méthane, 5% azote), l’analyse des fumées suivante a été obtenue: dioxyde de carbone 9,1%, monoxyde de carbone 0,2%, oxygène 4,6%, azote 86,1%, tous les pourcentages sont volumiques.
Calculez le pourcentage de débit d’air en excès (pourcentage supérieur à la stœchiométrique)
Solution
Réaction: CH4 + 2O2 = CO2 + 2H2O
Remarque: l’analyse des gaz de combustion est rapportée sur une base sèche, toute eau formée ayant été condensée. L’azote est le composant de liaison (ou de nœud).
Base: 100 moles, gaz de combustion secs; comme l’analyse des gaz de combustion est connue, les moles de chaque élément dans les gaz de combustion (flux de sortie) peuvent être facilement calculées et liées au débit alimentant le système.
Soit X la quantité de combustible (gaz naturel) pour 100 moles de gaz de combustion sec.
Bilan sur le carbone: moles de combustible = mole de gaz de combustion
0,95X = 9,1 + 0,2, d’où X = 9,79 mol
Bilan sur l’azote (composition de l’air O2: 21%, N2: 79%):
Soit Y le débit d’air pour 100 moles de gaz de combustion secs.
N2 dans l’air + N2 dans le combustible = N2 dans les fumées
0,79Y +0.05 . 9,79 = 86,1 d’où Y = 108,4 mol
Air stœchiométrique: D’après l’équation de réaction, 1 mol de méthane nécessite 2 mol d’oxygène, donc:
air stœchiométrique = 9,79. 0,95. 2 . (100/21) = 88,6 mol
Pourcentage d’air en excès =
((air fourni – air stœchiométrique) / air stœchiométrique)
. 100
= (108,4 – 88,6) /88,6 = 22 pour cent
Notez que nous avons simplifié le problème en négligeant le dioxyde de carbone présent dans l’air ambiant. D’après un exemple précédent, c’est 0,03%, c’est-à-dire 108,4. 0,00003 = 0,0325 mole pour 100 moles de gaz de combustion sec, soit environ une erreur d’un tiers d’un pour cent. Cela n’affecte pas de manière significative le calcul du pourcentage d’air en excès.
CONVERSION, SÉLECTIVITÉ ET RENDEMENT
Il est important de faire la distinction entre la conversion et le rendement. La conversion concerne les réactifs; rendement concerne les produits.
Conversion
La conversion est une mesure de la fraction du réactif qui réagit. Pour optimiser la conception du réacteur et minimiser la formation de sous-produits, la conversion d’un réactif particulier est souvent inférieure à 100%. Si plusieurs réactifs sont utilisés, le réactif par rapport auquel la conversion est calculée doit être spécifié.
La conversion est définie par l’expression suivante:
Conversion = quantité de réactif consommée / quantité fournie
= ((quantité dans le flux d’alimentation) – (quantité dans le flux des produits)) / (quantité dans le flux d’alimentation)
Cette définition donne la conversion totale du réactif désigné en tous les produits.
Exemple:
Dans la fabrication du chlorure de vinyle (VC) par pyrolyse du dichloroéthane (DCE), la conversion du réacteur est limitée à 55% pour réduire la formation de carbone qui encrasse les tubes du réacteur.
Calculez la quantité de DCE introduite dans le réacteur pour produire 5000 kg/h de VC.
Solution
Base: 5000 kg/h VC (la quantité requise).
Réaction: C2H4Cl2 = C2H3Cl + HCl
Masses molaires: DCE 99, VC 62,5
kmol/h VC produit = 5000 / 62,5 = 80
À partir de l’équation stœchiométrique, 1 kmol de DCE produit 1 kmol de VC. Soit X DCE alimenté en kmol / h:
Taux de conversion = 55 = (80 / X). 100
X = 80 / 0,55 = 145,5 kmol/h
Dans cet exemple, la petite perte de DCE transformée en carbone et autres produits a été négligée. Tout le DCE ayant réagi a été supposé être converti en VC.
Sélectivité
La sélectivité est une mesure de l’efficacité du réacteur à convertir le réactif en produit souhaité. C’est la fraction de la matière ayant réagi qui a été convertie en produit souhaité. Si aucun sous-produit n’est formé, la sélectivité est de 100%. Si des réactions secondaires se produisent et que des sous-produits se forment, la sélectivité diminue. La sélectivité est toujours exprimée comme la sélectivité du réactif A pour le produit B et est définie par l’équation suivante:
Sélectivité = moles de B formées / moles de B qui auraient pu se former si tout A réagissait pour donner B
= moles de B formées / (moles de A consommées. facteur stœchiométrique)
Facteur stœchiométrique = moles de B produites par mole de A réagi
dans l’équation stœchiométrique de réaction
La sélectivité est généralement améliorée en faisant fonctionner le réacteur à de faibles conversions. À une conversion élevée, le réacteur a de faibles concentrations d’au moins un réactif et des concentrations élevées de produits, de sorte que les réactions qui forment des sous-produits sont plus susceptibles de se produire.
Les réactifs qui ne sont pas convertis dans le réacteur peuvent être récupérés et recyclés.
Les réactifs qui sont convertis en sous-produits ne peuvent généralement pas être récupérés et les sous-produits doivent être purifiés pour être vendus ou éliminés comme déchets (voir plus loin). Les conditions optimales du réacteur favorisent ainsi habituellement une faible conversion du réacteur pour donner une sélectivité élevée pour les produits désirés lorsque tous ces coûts sont pris en compte.
Rendement:
Le rendement est une mesure de la performance d’un réacteur ou d’une usine. Plusieurs définitions différentes du rendement sont utilisées, et il est important d’indiquer clairement la base de tout nombre de rendement. Cela n’est souvent pas fait lorsque les rendements sont cités dans la littérature, et le jugement doit être utilisé pour décider de ce qui était prévu.
Le rendement en produit B de l’alimentation A est défini par:
Rendement = moles de B formées / moles de A fournies. facteur stœchiométrique
Pour un réacteur, le rendement est le produit de la conversion et de la sélectivité:
Rendement de la réaction = Conversion. Sélectivité
= (moles A consommées / moles A alimentées). (moles B formées
/ (moles A consommées. facteur stœchiométrique))
Avec les réacteurs industriels, il est nécessaire de faire la distinction entre le «rendement de réaction» (rendement chimique), qui comprend uniquement les pertes chimiques vers les produits secondaires; et le «rendement du réacteur» global, qui comprend également les pertes physiques, telles que les pertes par évaporation dans le gaz d’évacuation.
Si la conversion est proche de 100%, il peut ne pas valoir la peine de séparer et de recycler le matériau n’ayant pas réagi; le rendement global du réacteur inclurait alors la perte de matière n’ayant pas réagi. Si le matériau n’ayant pas réagi est séparé et recyclé, le rendement global repris dans le réacteur et l’étape de séparation comprendrait toutes les pertes physiques de l’étape de séparation.
Le rendement de l’usine est une mesure de la performance globale de l’usine et comprend toutes les pertes chimiques et physiques.
Rendement de l’usine (appliqué à l’usine entière ou à n’importe quel stade) =
moles de produit fabriquées /
(moles de réactif fournies au procédé désigné. facteur stœchiométrique)
Lorsque plus d’un réactif est utilisé, ou plus d’un produit est fabriqué, il est essentiel que le produit et le réactif auxquels se réfère le calcul de rendement soient clairement indiqués.
Le rendement de l’usine de B à partir de A est le produit de la sélectivité du réacteur de la charge A pour le produit B et de l’efficacité de séparation (récupération) de chaque étape de séparation qui manipule le produit B ou le réactif A.
Exemple:
Dans la production d’éthanol par hydrolyse de l’éthylène, l’éther diéthylique est produit comme sous-produit. Une composition de courant d’alimentation typique est 55% d’éthylène, 5% d’inertes, 40% d’eau; et courant de produit: 52,26% d’éthylène, 5,49% d’éthanol, 0,16% d’éther, 36,81% d’eau, 5,28% d’inertes. Calculez la sélectivité de l’éthylène pour l’éthanol et pour l’éther.
Solution
Réactions: C2H4 + H2O = C2H5OH (a)
2C2H5OH = (C2H5)2O + H2O (b)
Base: 100 moles d’alimentation (calcul plus facile que l’utilisation du flux de produit)
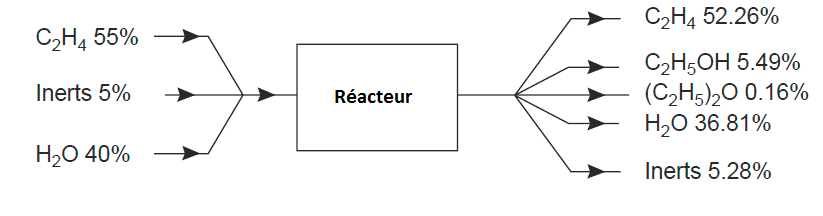
Remarque: le flux d’inertes sera constant, car ils ne réagissent pas; et il peut ainsi être utilisé pour calculer les autres flux à partir des compositions.
Flux d’alimentation
éthylène 55 mol
inertes 5 mol
eau 40 mol
Flux de produits
éthylène = (52, 26/5, 28). 5 = 49,49 mol
éthanol = (5, 49/5, 28). 5 = 5,20 mol
éther = (0, 16/5, 28). 5 = 0,15 mol
Quantité d’éthylène ayant réagi = 55,0 – 49,49 = 5,51 mol
Sélectivité de l’éthylène pour l’éthanol = (5, 20/(5,51 . 1,0)) . 100 = 94,4%
Comme 1 mole d’éthanol est produite par mole d’éthylène, le facteur stœchiométrique est de 1.
Sélectivité de l’éthylène pour l’éther = 0,15 / (5,51. 0,5). 100 = 5,44%
Le facteur stœchiométrique est de 0,5, car 2 moles d’éthylène produisent 1 mole d’éther.
Notez que la conversion de l’éthylène, en tous les produits, est donnée par
Conversion = (moles alimentées – moles sortantes)/ mols alimentées = ((55 – 49,49) / 55). 100
= 10 pour cent
La sélectivité basée sur l’eau pourrait également être calculée mais ne présente aucun intérêt réel, car l’eau est relativement peu coûteuse par rapport à l’éthylène. L’eau est clairement introduite dans le réacteur en excès considérable.
Le rendement en éthanol à base d’éthylène est
Rendement de la réaction = (5,20 / (55 . 1,0)). 100 = 9,45%
Exemple:
Dans la chloration de l’éthylène pour produire du dichloroéthane (DCE), la conversion de l’éthylène est de 99,0%. Si 94 moles de DCE sont produites pour 100 moles d’éthylène ayant réagi, calculez la sélectivité et le rendement global par rapport à l’éthylène. L’éthylène n’ayant pas réagi n’est pas récupéré.
Solution
Réaction: C2H4 + Cl2 = C2H4Cl2
Le facteur stœchiométrique est 1.
Sélectivité = (moles de DCE produites / (moles d’éthylène ayant réagi . 1)) .100
= (94/100). 100 = 94%
Rendement global (y compris les pertes physiques) =
(moles de DCE produites / (moles d’éthylène alimentées. 1)). 100
Par conséquent, 99 moles d’éthylène sont mises à réagir pour 100 moles d’alimentation, donc:
Rendement global = (94/100). (99/100) = 93,1%
Notez que nous obtenons la même réponse en multipliant la sélectivité (0,94) et la conversion (0,99).
Le principal sous-produit de ce procédé est le trichloroéthane.
Sources de données de conversion, de sélectivité et de rendement.
S’il y a une formation minimale de sous-produits, alors les coûts du réacteur (volume, catalyseur, chauffage, etc.) peuvent être mis en compromis avec les coûts de séparation et de recyclage des réactifs non convertis pour déterminer la conversion optimale du réacteur. Plus fréquemment, la sélectivité des charges les plus chères pour le produit souhaité est inférieure à 100%, et les coûts des sous-produits doivent également être pris en compte. L’optimisation du réacteur nécessite alors une relation entre la conversion du réacteur et la sélectivité, non seulement pour le produit principal, mais pour tous les sous-produits qui se forment en quantité suffisante pour avoir un impact sur les coûts du procédé.
Dans des cas simples, lorsque le nombre de sous-produits est petit, il peut être possible de développer un modèle mécaniste de la cinétique de réaction qui prédit la vitesse de formation du produit principal et des sous-produits. Si un tel modèle est adapté à des données expérimentales sur une gamme suffisamment large de conditions opératoires du procédé, il peut être utilisé pour l’optimisation de ce dernier.
Le développement de modèles de cinétique réactionnelle est décrit dans la plupart des manuels d’ingénierie de réaction. Voir, par exemple, Levenspiel (1998), Froment et Bischoff (1990) et Fogler (2005).
Dans les cas où la réaction passe rapidement à l’équilibre, les rendements sont facilement estimés en tant que rendements d’équilibre. Dans ces circonstances, les seules possibilités d’optimisation du procédé sont de changer la température, la pression ou la composition de la charge, de manière à obtenir un mélange d’équilibre différent. Le calcul de l’équilibre de réaction est facilement réalisé à l’aide de programmes commerciaux de simulation des procédés.
Lorsque le nombre de composants ou de réactions est trop grand ou que le mécanisme est trop complexe pour être déduit avec une certitude statistique, des modèles de surfaces de réponse peuvent être utilisés. Des méthodes pour la conception statistique des expériences peuvent être appliquées, réduisant la quantité de données expérimentales qui doivent être collectées pour former une corrélation statistiquement significative de sélectivité et de rendement aux principaux paramètres opératoires du procédé. Voir Montgomery (2001) pour une bonne introduction à la conception statistique des expériences.
Dans les premières étapes de la conception, l’ingénieur concepteur n’aura souvent ni surface de réponse, ni modèle mécaniste détaillé de la cinétique de réaction. Peu d’entreprises sont prêtes à consacrer un laboratoire ou une usine pilote et le personnel nécessaire à la collecte des données de la cinétique de réaction jusqu’à ce que la direction soit convaincue que le procédé étudié est économiquement attrayant. Une conception est donc nécessaire avant que l’ensemble de données nécessaires ne soit collecté. Dans de telles circonstances, l’ingénieur de conception doit sélectionner les conditions optimales du réacteur à partir des données disponibles. Cette première estimation du rendement du réacteur peut provenir de quelques points de données collectés par un chimiste ou tirés d’un brevet ou d’une recherche documentée. L’utilisation des données issues des brevets est abordée plus tard.
Dans l’objectif de compléter une conception, une seule estimation du rendement du réacteur est nécessaire. Des données de rendement supplémentaires prises sur une plus large gamme de conditions opératoires donnent au concepteur une meilleure capacité à optimiser correctement la conception.
PROCESSUS DE RECYCLAGE
Les procédés dans lesquels un flux d’écoulement est renvoyé (recyclé) à une étape antérieure de la séquence de traitement sont fréquemment utilisés. Si la conversion d’un réactif précieux dans un procédé réactionnel est sensiblement inférieure à 100%, le réactif n’ayant pas réagi est généralement séparé et recyclé. Le retour du reflux en tête d’une colonne de distillation est un exemple de procédé avec recyclage et dans lequel il n’y a pas de réaction.
Dans les calculs de bilans matière, la présence de flux de recyclage rend la tache plus difficile.
Sans recyclage, les bilans sur une série d’étapes de traitement peuvent être effectués séquentiellement, en prenant chaque unité à son tour; les flux calculés d’une unité deviennent les flux alimentant la suivante. Si un flux de recyclage est présent, alors au point où le recyclage est renvoyé, le flux ne sera pas connu car il dépendra des flux en aval non encore calculés. Si le flux de recyclage n’est pas connu, la séquence des calculs ne peut pas être poursuivie tant que le flux de recyclage peut être déterminé.
Deux approches pour résoudre les problèmes de recyclage sont possibles:
A. La méthode du cut-and-try («déchirer»). Les débits des flux de recyclage peuvent être estimés et les calculs sont poursuivis jusqu’au point où le recyclage est calculé. Les débits estimés sont ensuite comparés à ceux calculés et une meilleure estimation est ré-effectuée. La procédure se poursuit jusqu’à ce que la différence entre les débits estimés et calculés se situe dans une tolérance acceptable.
B. La méthode formelle et algébrique. La présence de recyclage implique que certaines des équations de bilan massique doivent être résolues simultanément. Les équations sont établies avec les débits de recyclage comme des inconnues et résolues à l’aide de méthodes standards pour la résolution d’équations simultanées. Avec des problèmes simples qui n’ont qu’une ou deux boucles de recyclage, le calcul peut souvent être simplifié par une sélection minutieuse de la base de calcul et des limites du système. Ceci est illustré dans l’exemple qui suit. La solution aux problèmes de bilan matière plus complexes impliquant plusieurs boucles de recyclage est abordée plus tard.
Exemple:
Le schéma synoptique montre les principales étapes du procédé de production de chlorure de vinyle à partir d’éthylène. Chaque bloc représente un réacteur et plusieurs autres unités de traitement. Les principales réactions sont:
Bloc A, chloration
C2H4 + Cl2 = C2H4Cl2, rendement sur éthylène 98%
Bloc B, oxyhydrochloration
C2H4 + 2HCl + 0,5O2 = C2H4Cl2 + H20 rendements sur éthylène 95%, sur HCl 90%
Bloc C, pyrolyse
C2H4Cl2 (DCE)= C2H3Cl (VC) + HCl, rendement sur DCE 99%, sur HCl 99,5%
Le HCl issu de l’étape de pyrolyse est recyclé vers l’étape d’oxyhydrochloration. Le débit d’éthylène vers les réacteurs de chloration et d’oxyhydrochloration est ajusté pour que la production d’HCl soit en équilibre avec le besoin. La conversion dans le réacteur de pyrolyse est limitée à 55% et le dichloroéthane (DCE) n’ayant pas réagi est séparé et recyclé.
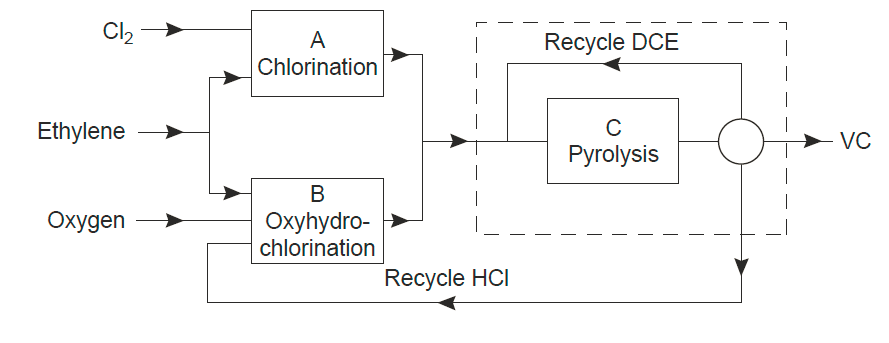
En utilisant les chiffres de rendement donnés, et en négligeant les autres pertes, calculer le débit d’éthylène vers chaque réacteur et le débit de DCE vers le réacteur de pyrolyse, pour un débit de production de 12 500 kg / h de chlorure de vinyle (VC).
Solution
Masses moléculaires: chlorure de vinyle 62,5; DCE 99,0; HCl 36,5.
VC par heure = 12500 / 62,5 = 200 kmol / h
Tracer une frontière du système autour de chaque bloc, enfermant le recyclage DCE dans la limite de l’étape C.
Prendre X le débit d’éthylène au bloc A et Y le débit au bloc B, et le HCl recyclé au bloc B: Z.
Ensuite, le total des moles de DCE produites = 0,98X + 0,95Y, compte tenu des rendements, et les moles de HCl produites dans le bloc C
= (0,98X + 0,95Y) 0,995 = Z (a)
Considérez les flux vers et depuis le bloc B
DCE
(Z) HCl
C2H4
O2
Bloquer
B
Le rendement en DCE basé sur HCl est de 90%, donc les moles de DCE produites = 0,5. 0,90.Z
Remarque: le facteur stœchiométrique est de 0,5 (2 moles HCl par mole DCE).
Le rendement en DCE basé sur l’éthylène est de 95%, donc:
0,5. 0,9Z = 0,95Y
Z = 0,95. 2Y / 0,9
La substitution de Z dans l’équation (a) donne
Y = (0,98X + 0,95Y). 0,995. (0,9 / (2. 0,95))
Y = 0,837.X (b)
Passant au bloc C, le VC total produit = 0,99. DCE total, donc:
0,99 (0,98X + 0,95Y) = 200 kmol / h
La substitution de Y à partir de l’équation (b) donne X = 113,8 kmol / h
et: Y = 0,837. 113,8 = 95,3 kmol / h
Recyclage du HCl à partir de l’équation (a)
Z = (0,98. 113,8 + 0,95. 95,3) 0,995 = 201,1kmol / h
Remarque: Rendement global sur éthylène = (200 / (113,8 + 95,3)). 100 = 96 pour cent
PURGE
Il est généralement nécessaire de purger une partie d’un flux de recyclage pour éviter l’accumulation de matières indésirables. Par exemple, si l’alimentation d’un réacteur contient des composants inertes qui ne sont pas séparés du courant de recyclage dans les unités de séparation, ces inertes s’accumuleraient dans le courant de recyclage jusqu’à ce que le courant soit finalement presque entièrement constitué d’inertes. Une partie du flux doit être purgée pour maintenir le niveau des inertes dans des limites acceptables. Une purge continue serait normalement utilisée. Dans des conditions d’équilibre:
Perte d’inertie lors de la purge = débit d’inertes dans le système
La concentration de tout composant dans le courant de purge est la même que celle dans le courant de recyclage au point où la purge est prélevée. Ainsi, le taux de purge requis peut être déterminé à partir de la relation suivante:
[Débit du flux d’alimentation]. [Concentration inerte du flux d’alimentation]
= [Débit du flux de purge]. [Concentration inerte de recyclage spécifiée (souhaitée)]
Exemple:
Dans la production d’ammoniac à partir d’hydrogène et d’azote, la conversion, basée sur l’une ou l’autre des matières premières, est limitée à 15%. L’ammoniac produit est condensé à partir du courant produit du réacteur (convertisseur) et les réactifs n’ayant pas réagi sont recyclés. Si l’alimentation contient 0,2% d’argon (provenant du procédé de séparation de l’azote), calculez le taux de purge requis pour contenir l’argon dans le flux de recyclage à 5,0%. Les pourcentages sont en volume.
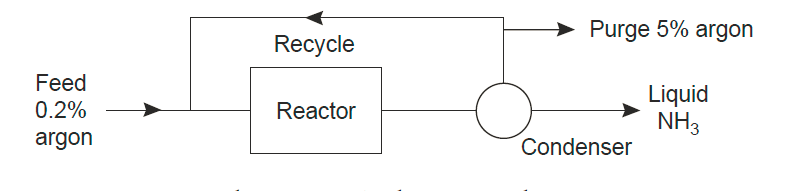
Solution
Base: 100 moles d’alimentation (le taux de purge sera exprimé en moles pour 100 moles d’alimentation, car le taux de production n’est pas donné).
Les pourcentages en volume sont considérés comme équivalents à mol%.
Système d’entrée d’argon en alimentation = 100. 0,2 / 100 = 0,2 mol.
Soit F le taux de purge pour 100 moles d’alimentation.
Débit d’argon en purge = F. 5/100 = 0,05 F.
En régime stationnaire, argon sortant = argon entrant: 0,05F = 0,2
F = 0,2 / 0,05 = 4
Purge requise: 4 moles pour 100 moles d’alimentation.
BYPASS
Un flux en écoulement peut être divisé et une partie détournée (contournée) autour de certaines unités.
Cette procédure est souvent utilisée pour contrôler la composition du flux ou la température.
Les calculs du bilan matière sur les procédés avec des flux bypassés sont similaires à ceux impliquant le recyclage, sauf que le flux est alimenté en avant au lieu d’en arrière. Cela rend généralement les calculs plus faciles qu’avec le recyclage.
CALCULS EN RÉGIME TRANSITOIRE
Tous les exemples de bilans matière précédents étaient des soldes à l’état d’équilibre: régime stationnaire. Le terme d’accumulation a été pris égal à zéro et les débits et les compositions des courants ne variaient pas avec le temps. Si ces conditions ne sont pas remplies, les calculs sont plus complexes. Les calculs à l’état d’équilibre (stationnaire) sont généralement suffisants pour les calculs des procédés (voir plus tard). Le comportement instable d’un procédé est important lorsque l’on considère le démarrage et l’arrêt de ce dernier, ainsi que sa réponse à des perturbations.
Les procédés par lots (batch) sont également des exemples de fonctionnement en régime instable (transitoire); bien que les besoins totaux en matières puissent être calculés en prenant un lot (batch) comme base de calcul, des bilans à l’état instable sont nécessaires pour déterminer les temps de réaction et de séparation.
La procédure de résolution des bilans en régime non établi consiste à établir des petits soldes sur un petit incrément de temps, ce qui donnera une série d’équations différentielles décrivant le procédé. Pour des problèmes simples, ces équations peuvent être résolues analytiquement. Pour les problèmes plus complexes, des méthodes informatiques sont utilisées. L’approche générale de la solution des problèmes à l’état transitoire est illustrée dans l’exemple qui suit. Le comportement des procédés dans des conditions non stationnaires est un sujet complexe et spécialisé (voir plus tard). Cela peut être important dans la conception d’un procédé lors de l’évaluation du comportement de ce dernier du point de vue de la sécurité et du contrôle. L’utilisation des bilans de matière dans la modélisation de processus complexes à l’état transitoire est discutée dans les livres de Myers et Seider (1976) et Henley et Rosen (1969).
Exemple
Un réservoir ‘de cale’ est installé dans un procédé de traitement d’effluents aqueux pour lisser les fluctuations de concentration du courant d’effluent. L’effluent alimentant le réservoir ne contient normalement pas plus de 100 ppm d’acétone. La concentration maximale admissible d’acétone dans le rejet d’effluent est fixée à 200 ppm. La capacité de travail du réservoir de décharge est de 500 m3 et il peut être considéré comme parfaitement mélangé. Le débit d’effluent est de 45 000 kg / h. Si la concentration d’acétone dans l’alimentation augmente soudainement à 1000 ppm, en raison d’un déversement dans l’usine de traitement, et reste à ce niveau pendant une demi-heure, la limite de 200 ppm dans le rejet d’effluent sera-t-elle dépassée?
Solution:
Base: incrément de temps Dt.
Pour illustrer la solution générale à ce type de problème, le bilan sera mis en place en symboles pour toutes les grandeurs puis en valeurs réelles pour cet exemple substituées.
Masse dans le réservoir = M,
Débit = F,
Concentration initiale dans le réservoir = C0,
Concentration au temps t après l’augmentation de la concentration d’alimentation = C,
Concentration dans la charge d’effluent = C1,
changement de concentration au fil du temps Dt : DC,
concentration moyenne dans le réservoir pendant l’incrément de temps = Cm.
Puis, comme il n’y a pas de génération dans le système, le bilan matière général s’écrit:
Entrée – Sortie = Accumulation
Bilan matière sur l’acétone.
Remarque: Comme le réservoir est considéré comme parfaitement mélangé, la concentration de sortie sera la même que la concentration dans le réservoir.
Acétone in – Acetone out = Acétone accumulée dans le réservoir
F.C1.Dt – F.Cm.Dt = M. (C + DC) – M.C
F. (C1 – Cm) = M. (DC / Dt)
Prendre la limite, comme Dt tend vers 0
DC / Dt = dC / dt et Cm = C
F (C1 – C) = M. (dC / dt)
Après intégration:
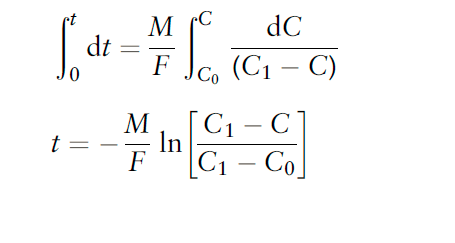
En remplaçant les valeurs de l’exemple et en notant que la concentration de sortie maximale se produit à la fin de la période d’une demi-heure de concentration d’entrée élevée:
t = 0,5h
C1 = 1 000 ppm
C0 = 100 ppm (valeur normale)
M = 500m3 = 500000 kg
F = 45 000 kg / h
0,5 = – (500000/45000) .ln ((1000 -C) / (1000 -100))
0,045 = -ln ((1000 -C) / 900)
exp (-0,045) .900 = 1000 – C
C = 140 ppm
Ainsi, la concentration maximale autorisée n’est pas dépassée.
PROCÉDURE GÉNÉRALE POUR LES PROBLÈMES D’ÉQUILIBRE MATÉRIEL
La meilleure façon d’aborder un problème dépendra des informations fournies, des informations demandées du bilan, et les contraintes qui découlent de la nature du problème. Il n’est pas possible de donner la meilleure méthode globale de solution pour couvrir tous les possibles
problèmes. La procédure étape par étape suivante est donnée comme une aide à la solution efficace aux problèmes de bilan matière. La même approche générale peut être utile utilisé pour organiser la solution des bilans énergétiques et autres problèmes de conception.
Procédure
Étape 1. Dessinez un schéma synoptique du procédé.
Montrez chaque étape significative sous forme de bloc, lié par des lignes et des flèches pour montrer les connexions des flux et leurs directions.
Étape 2. Dressez la liste des données disponibles.
Affichez sur le diagramme les débits (ou quantités) connus et les compositions de flux.
Étape 3. Répertoriez toutes les informations requises du bilan.
Étape 4. Décidez des limites du système (voir plus haut).
Étape 5. Écrivez les réactions chimiques impliquées pour les principaux produits et sous-produits.
Étape 6. Notez toutes les autres contraintes, telles que les compositions de flux spécifiées, les azéotropes, l’équilibre de phase ou de réaction, les substances liées ou ‘nœuds’ (voir plus haut).
L’utilisation des relations d’équilibre de phases et d’autres contraintes dans la détermination des compositions et des débits est discutée plus en détail (voir en bas).
Étape 7. Notez les compositions et les débits qui peuvent être approximés.
Étape 8. Vérifiez le nombre d’équations de conservation (et autres) qui peuvent être écrites et comparez-le avec le nombre d’inconnues. Décidez quelles variables doivent être des variables de conception. (voir en haut)
Cette étape ne serait utilisée que pour des problèmes complexes.
Étape 9. Décidez de la base des calculs (voir en haut)
L’ordre dans lequel ces étapes sont effectuées peut être modifié en fonction du problème.
